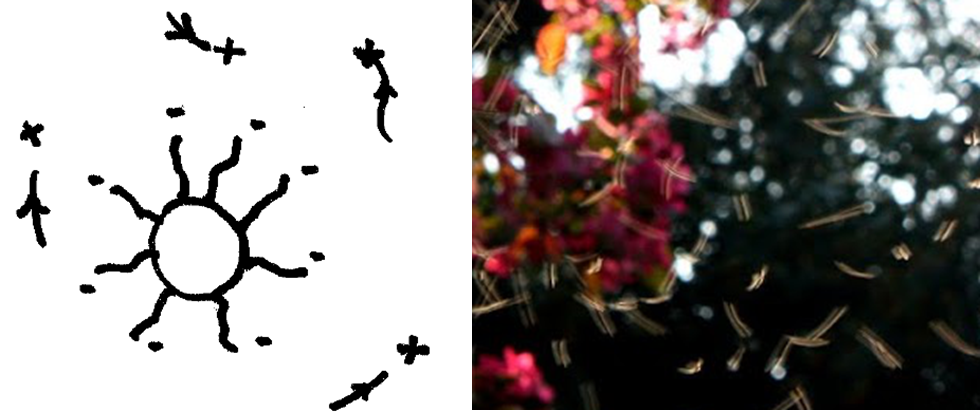Les cristaux sont des empilements réguliers d’atome. Or vu de loin, un atome n’est autre qu’une boule, et un cristal un empilement de boules, on prend souvent les oranges des étalages pour exemple, pour changer voici des reine-claudes:
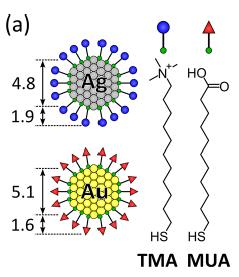
Bien sûr la différence entre cet empilement et un vrai cristal est que les reines-claudes roulent lorsqu’on incline le cageot: il n’y a aucune cohésion. Dans le cristal, de sel de Guérande par exemple, ce sont les charges électrostatiques opposées (Na+ et Cl-) des ions qui le composent qui assurent ce rôle. Pour trouver une analogie plus fidèle, il faut donc apporter un peu de cohésion, un peu de glu: c’est ce que nous avons fait avec K. Bishop de l’Université de Pennsylvanie et B. Grzybowski de la Northwestern University, en considérant comme constituants élémentaires du cristal non plus l’ion, mais des nanoparticules de charges opposées. On obtient celles-ci par précipitation de métaux nobles (or et argent) dans des mélanges non miscibles (type eau-huile), donnant autant de petites billes d’or et d’argent qu’il y a de gouttes dans l’émulsion. On recouvre ensuite chacune des billes avec un surfactant, une molécule dont une extrémité va s’accrocher à l’or (ou l’argent) et l’autre présenter une charge. Le résultat ressemble schématiquement à cela:
Les nanoparticules font une dizaine de nanomètres de diamètre, soit 20-100 fois plus qu’un ion (qui se mesure plutôt en dixième de nanomètre). On peut ainsi obtenir deux fioles de produit, l’une avec des nanoparticules moins et l’autre avec les plus. Bien sûr, aucune des fioles n’est chargée en soit : le contrepoids en charge électrique est assuré par les bien nommés contre-ions, qui ont fait le voyage avec le surfactant, et orbitent à proximité des nanoparticules chargées un peu comme un nuage de mouche autour d’un fruit bien mûr.
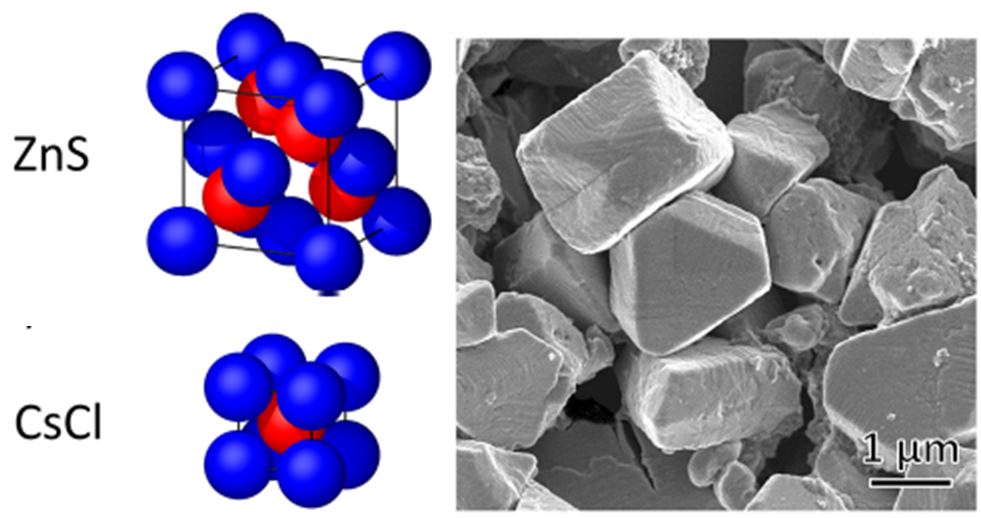
Très loin de la bille, les contre-ions masquent totalement la charge qu’elle porte, on dit qu’ils écrantent; il faut se rapprocher près (en deçà de la longueur de Debye) pour commencer à sentir le champ électrique d’une nanoparticule. Lorsqu’on mélange la fiole + avec la fiole -, on s’y attendait, les billes cristallisent. Pour des billes de tailles égales et de charges égales (mais opposées) l’arrangement le plus compact, le plus favorable devrait être celui du chlorure de césium (CsCl). L’expérience montre qu’on obtient en réalité une structure différente, plus lâche, celle du diamant. les chimistes (G. Stoyev, XXXX) du laboratoire de M. Grzybowski venaient de produire des diamants d’or et d’argent.
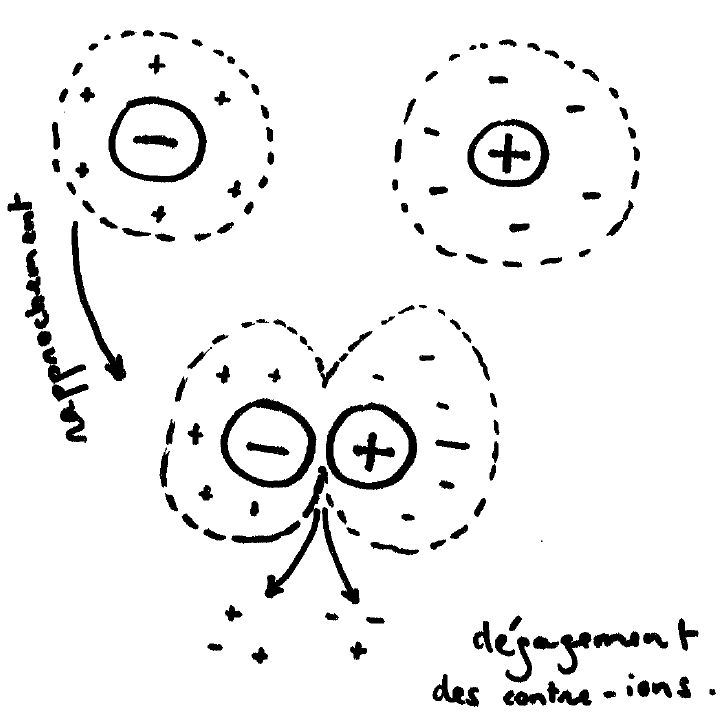
Ce fût le point de départ de nos recherches. Pour saisir pourquoi une assemblée de bille s’organise en diamant, il nous a fallu comprendre d’abord comment deux billes interagissent l’une avec l’autre. De loin, elles sont écrantées et n’interagissent pas. Au fur et à mesure qu’on les rapproche, la charge globale de l’ensemble des deux billes va progressivement tendre vers zéro, les contre-ions ont de moins en moins de charges à compenser et regagnent la solution : le rapprochement s’accompagne d’un dégagement d’ions.
Ce faisant , le système est plus dispersé (une fraction des ions n’orbite plus autour des billes), on dit qu’il a gagné en entropie, ce qui rend le rapprochement des nanoparticules d’autant plus favorable. Dans le cas d’un cristal, on est en présence d’un grand nombre de billes. Si les billes ont exactement les même charges, les contre-ions sont totalement expulsés de la maille, l’équilibre des charges est assuré par la compensation des billes moins et des billes plus. Cependant s’il y a un petit déséquilibre de taille ou de charge entre les billes moins et les billes plus, celui-ci va être neutralisé par les contre-ions, qui se logent dans les espaces interstitiels. On aboutit à un système mixte où les charges sont à la fois portées par les billes et par une mer d’ions dans laquelle baigne le cristal.
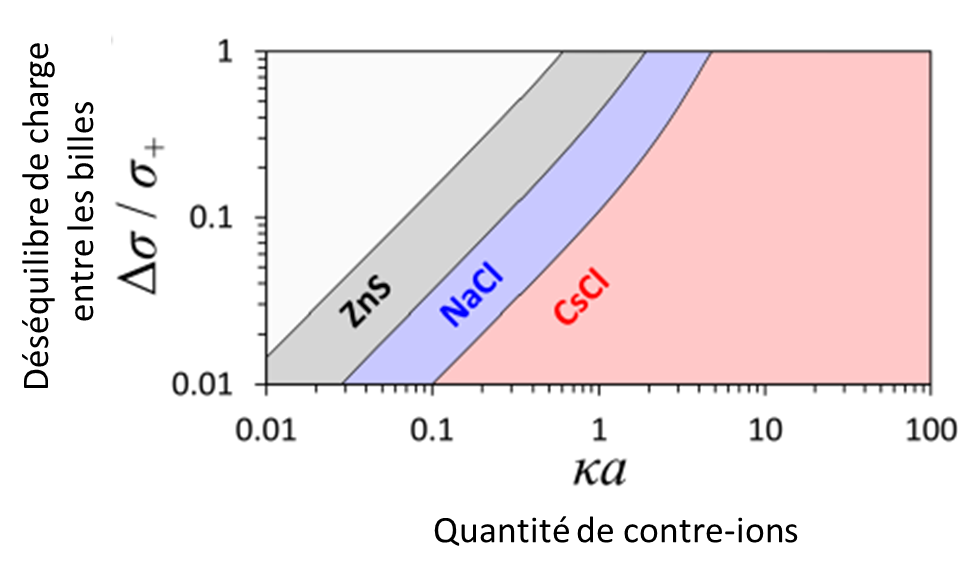
Avec K. Bishop nous avons pu montré que les espaces interstitiels plus importants du diamant conféraient plus de liberté, d’entropie aux contre-ions, ce qui rend cette structure favorable comparée aux niches compactes du CsCl, comme on le voit sur ce diagramme de phase:
Ceci semble fournir une explication raisonnable des résultats de nos collègues chimistes et donne des bases théoriques pour la conception d’un diamant colloïdale (pas celui-ci mais celui-là). Le papier complet est ici.